MDCG 2021‑24 Rev.1 — 医疗器械分类发生了什么变化?
1。背景和目标
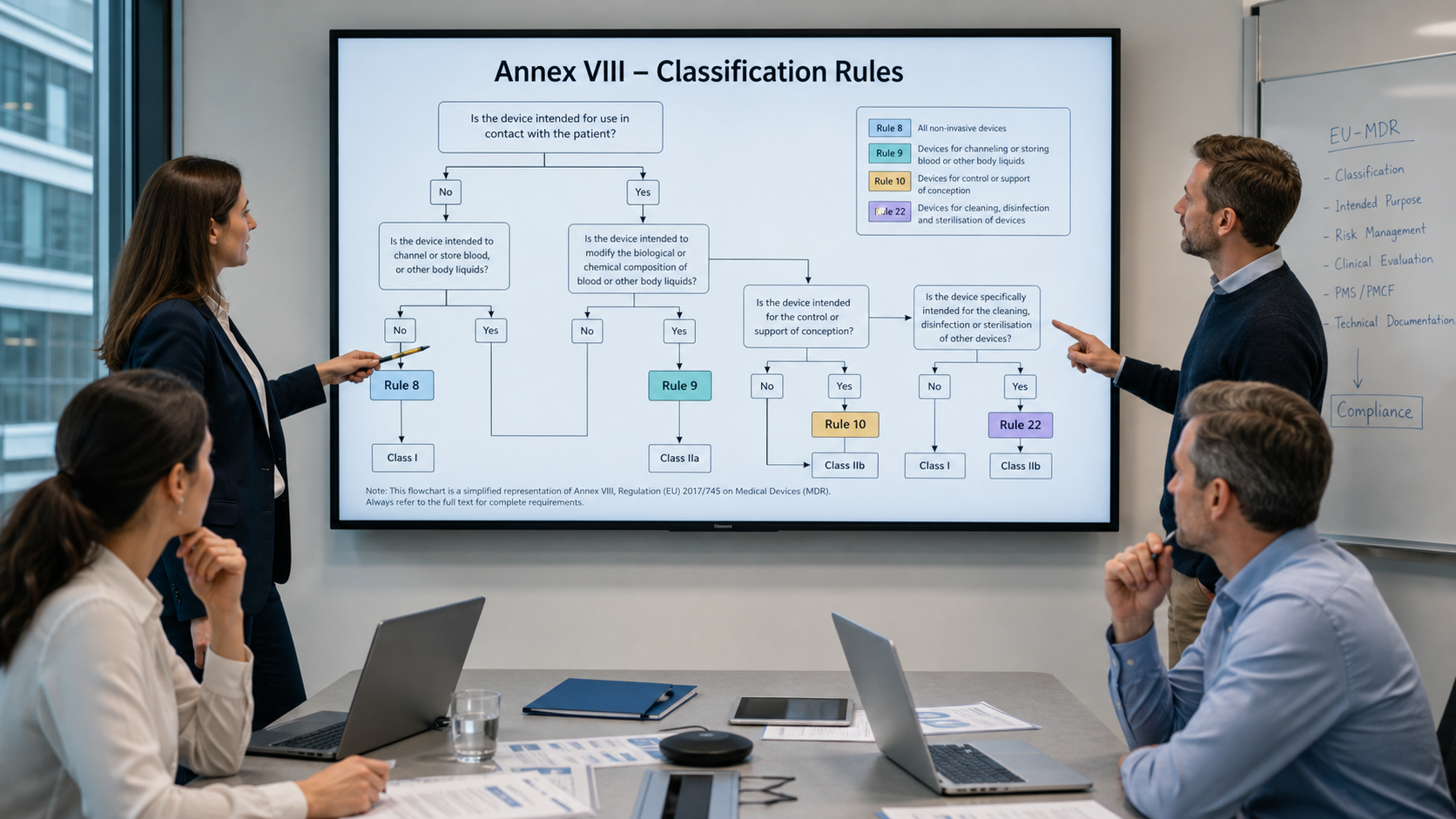
指南MDCG 2021‑24帮助制造商、申报机构和其他行为者一致地适用(欧盟)2017/745号法规(MDR)附件八中规定的分类规则。2026年4月发布的修订版1(MDCG 2021-24 Rev.1)在多个地方澄清了这些规则的解释,并补充了有关典型边缘案例的实用信息。
将设备归类为I、IIa、IIb或III类对于进一步的合规性评估流程、临床要求和上市后工作至关重要。分类错误可能导致批准过程的延迟或公告机构和当局的投诉。
2。MDCG 2021‑24 Rev.1 中的相关变化
修订主要侧重于澄清和完善与实践相关的例子。以下情况尤其受到影响:
- 植入式设备的定义和临床干预一词
- 应用分类规则的语言版本(仅关注 “产品” 而不是 “设备”)
- 关于规则2、8、9、10、12、16和22的表格和实用信息
对于日常练习,这特别意味着:
- 更精确地区分产品组和相应的风险类别
- 对临界病例的额外解释,特别是植入式、主动和复杂系统的解释
- 更清楚地将附件十六的产品纳入分类逻辑
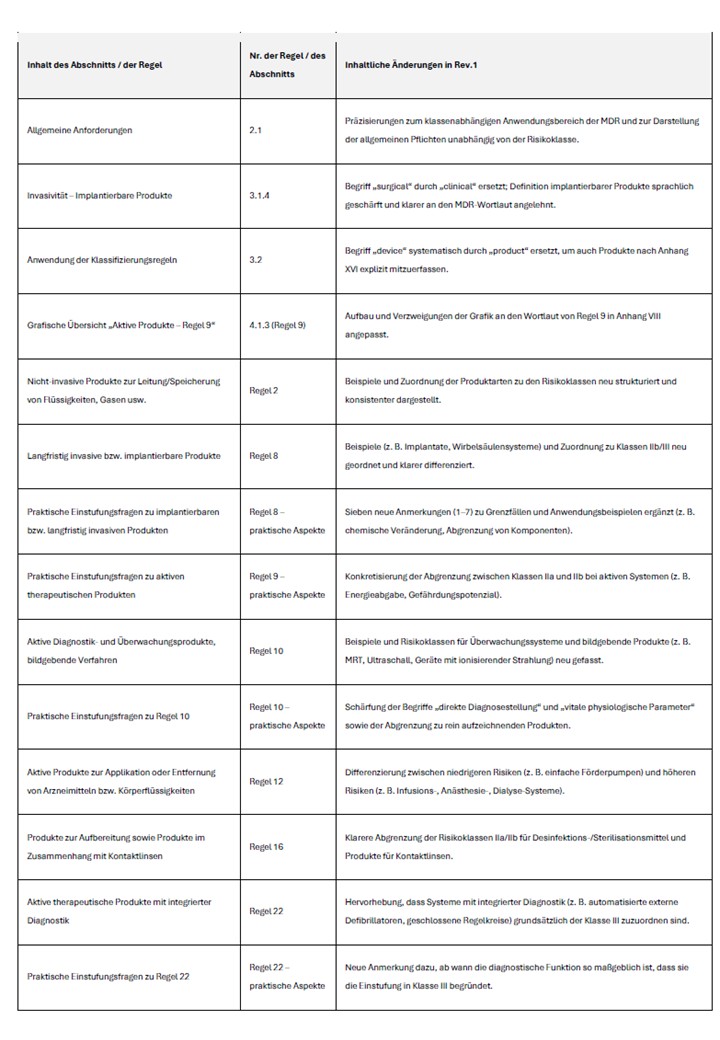
3.变更内容概述
下表概述了对修订版1的主要实质性调整。它适合作为对现有分类决定进行内部审查的起点。
4。给制造商和公告机构的建议
对于医疗器械和附件十六设备的制造商,建议在以下情况下专门审查现有分类:
- 带有可植入组件或长期侵入性使用的产品
- 具有大量能量输出的主动治疗系统
- 主动诊断和监测设备,尤其是在进行直接诊断时
- 具有集成诊断功能的复杂系统(例如闭环系统、AED)
具体而言,公司应至少调整以下文件和流程:
- 分类指南和工作说明 (SOP)
- 监管事务、开发和临床团队的培训材料
- 内部决策工具(例如分类矩阵、工具、清单)
来源
医疗器械协调小组 (MDCG): 医疗器械分类指南。MDCG 2021‑24,2021 年版本。
医疗器械协调小组 (MDCG): 医疗器械分类指南。MDCG 2021‑24 Rev.1,2026 年 4 月。
对于研究公司而言,更精确的MDCG指南为从一开始就使分类策略、研究设计和临床开发计划更具体地与MDR要求保持一致提供了机会,从而使审批流程更加可预测和高效。
这对你来说有趣吗? 联系我们 请随时联系我们进行初步咨询!
图标来源
目录
展示您的产品的医疗益处
凭借我们多年的经验和专业知识,我们提供有效的解决方案,以展示您的产品的医疗益处。
从临床前和临床研究的构思到实施,我们为您提供量身定制的服务。
了解 MEDIACC 如何帮助您获得产品退款。
