MDCG 2021‑24 Rev.1 – Was ändert sich bei der Klassifizierung von Medizinprodukten?
1. Hintergrund und Zielsetzung
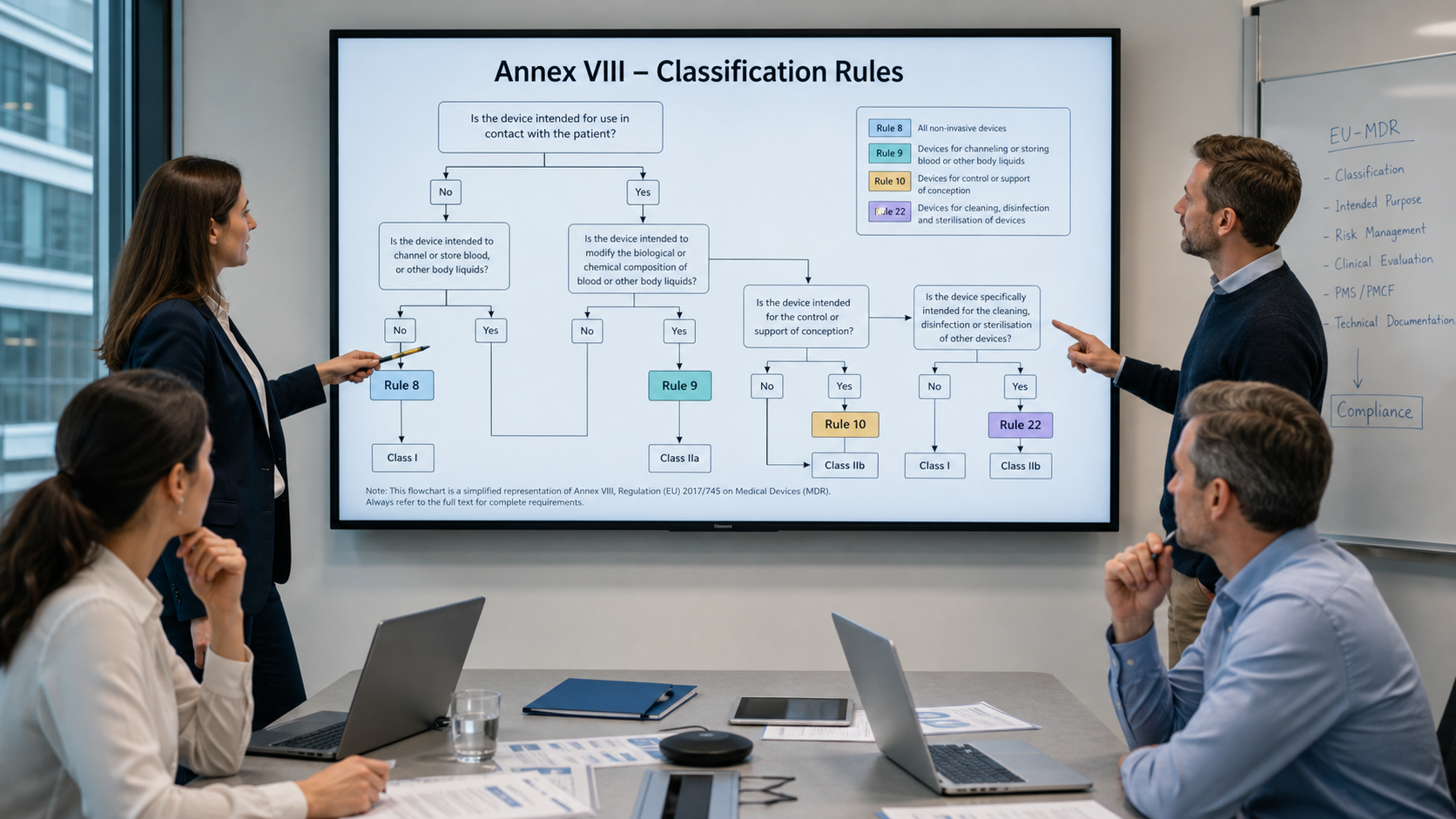
Die Leitlinie MDCG 2021‑24 unterstützt Hersteller, Benannte Stellen und andere Akteure dabei, die Klassifizierungsregeln des Anhangs VIII der Verordnung (EU) 2017/745 (MDR) einheitlich anzuwenden. Die im April 2026 veröffentlichte Revision 1 (MDCG 2021‑24 Rev.1) präzisiert an mehreren Stellen die Auslegung dieser Regeln und ergänzt praktische Hinweise zu typischen Grenzfällen.
Die Einstufung eines Produkts in die Klassen I, IIa, IIb oder III ist für das weitere Konformitätsbewertungsverfahren, die klinischen Anforderungen sowie den Aufwand in der Post‑Market‑Phase von zentraler Bedeutung. Fehler in der Klassifizierung können zu Verzögerungen im Zulassungsprozess oder zu Beanstandungen durch Benannte Stellen und Behörden führen.
2. Relevante Änderungen in MDCG 2021‑24 Rev.1
Die Revision konzentriert sich vor allem auf Klarstellungen und auf die Nachschärfung praxisrelevanter Beispiele. Besonders betroffen sind:
- die Definition implantierbarer Produkte und der Begriff der klinischen Intervention
- die sprachliche Fassung zur Anwendung der Klassifizierungsregeln (Fokus auf „product“ statt ausschließlich „device“)
- Tabellen und praxisbezogene Hinweise zu den Regeln 2, 8, 9, 10, 12, 16 und 22
Für die tägliche Praxis bedeutet das vor allem:
- eine präzisere Abgrenzung von Produktgruppen zu den jeweiligen Risikoklassen
- zusätzliche Erläuterungen zu Grenzfällen, insbesondere bei implantierbaren, aktiven und komplexen Systemen
- eine klarere Einbindung von Produkten nach Anhang XVI in die Klassifizierungslogik
3. Übersicht der geänderten Inhalte
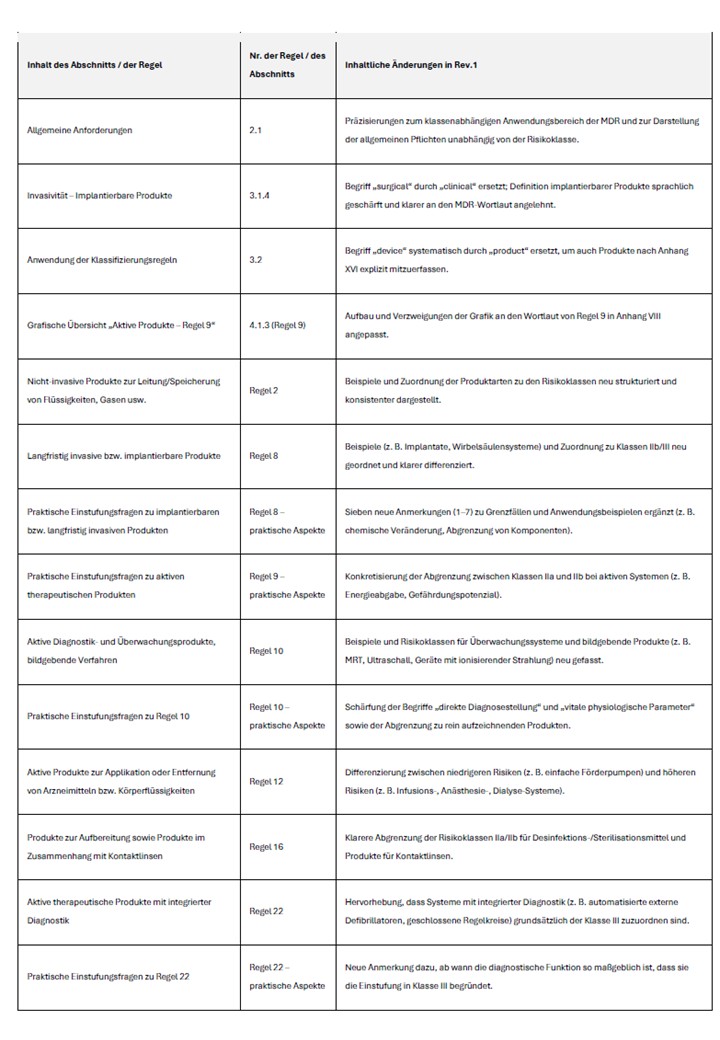
Die folgende Tabelle fasst die wesentlichen inhaltlichen Anpassungen der Revision 1 zusammen. Sie eignet sich als Ausgangspunkt für eine interne Überprüfung bestehender Klassifizierungsentscheidungen.
4. Empfehlungen für Hersteller und Benannte Stellen
Für Hersteller von Medizinprodukten und Annex‑XVI‑Produkten empfiehlt es sich, die bestehende Klassifizierung in folgenden Fällen gezielt zu überprüfen:
- Produkte mit implantierbaren Komponenten oder langfristig invasiver Anwendung
- aktive therapeutische Systeme mit signifikanter Energieabgabe
- aktive Diagnostik‑ und Überwachungsgeräte, insbesondere bei direkter Diagnosestellung
- komplexe Systeme mit integrierter Diagnostik (z. B. geschlossene Regelkreis‑Systeme, AEDs)
Konkret sollten unternehmensseitig mindestens folgende Dokumente und Prozesse angepasst werden:
- Klassifizierungs‑Richtlinien und Arbeitsanweisungen (SOPs, Work Instructions)
- Schulungsunterlagen für Regulatory Affairs, Entwicklung und klinische Teams
- interne Entscheidungshilfen (z. B. Klassifizierungs‑Matrizen, Tools, Checklisten)
Quellen
Medical Device Coordination Group (MDCG): Guidance on classification of medical devices. MDCG 2021‑24, Fassung 2021.
Medical Device Coordination Group (MDCG): Guidance on classification of medical devices. MDCG 2021‑24 Rev.1, April 2026.
Für forschende Unternehmen eröffnet die präzisere MDCG‑Guidance die Chance, Klassifizierungsstrategie, Studiendesigns und klinische Entwicklungspläne von Anfang an zielgerichteter an die MDR‑Anforderungen auszurichten und damit Zulassungsprozesse planbarer und effizienter zu gestalten.
Das ist für Sie interessant? Kontaktieren Sie uns gerne für ein erstes Beratungsgespräch!
Zeigen Sie den medizinischen Nutzen Ihres Produkts
Mit unserer langjährigen Erfahrung und Expertise bieten wir effektive Lösungen, um den medizinischen Nutzen Ihres Produktes zu zeigen.
Von der Konzeption bis zur Durchführung von präklinischen und klinischen Studien unterstützen wir Sie mit maßgeschneiderten Dienstleistungen.
Erfahren Sie, wie MEDIACC Ihnen zur Erstattungsfähigkeit Ihrer Produkte helfen kann.
